|
글리코믹스연구실 (지도교수: 도수일) |
미생물 유전학 연구실 (지도교수: 이창한) |
세포분화 연구실 (지도교수: 김혜선) |
생명정보학 및 유전체 연구실 (지도교수: 박대찬) |
분자생물학 연구실 (지도교수: 문은표) |

본 연구실은 포유류 글라이코믹스(Mammalian cell glycomics) 실험을 진행하고 있는 Functional Glycomics 실험실로서 세포수준 및 분자수준에서 당단백질 Glycoproteins 및 복합당질 Glycoconjugates 의 다양한 기능과 구조를 규명하는 최신연구들을 수행하고 있다. 특별히 인체 선천면역 방어기전에 관련된 당단백질의 기능해석과 암질환 및 알츠하이머와 같은 뇌신경질환에서 당단백질의 작용기전을 규명하고 있다. DNA와 RNA를 분석하는 분자생물학기술은 물론 PCR 증폭, 동물세포 배양, HPLC 분석, 당단백질 전기영동 및 Western blotting등 다양한 생물학적, 생화학적 기법을 이용하여 인체질환과 관련된 핵심적인 복합당질 분석 및 당단백질 작용점을 분석하는 실험들을 진행하고 있다. 또한 인체질환 관련 당단백질 작용점에 대한 작용기전의 규명을 위해 동물을 이용한 in vivo 준 임상실험도 병행해서 수행하고 있으며 최종 당단백질 작용점을 타겟하는 당의약(Glyco-Drug) 개발을 위한 당의과학 실험을 진행하고 있다.

미생물은 지구상에서 가장 오래된 생명체이자, 인간의 생명 유지에 직간접적으로 영향을 주는 매우 중요한 생명체 이다. 미생물은 다양한 자연환경이나 인간의 신체 내에서 다양한 스트레스에 노출되게 되는데, 많은 스트레스 물질들이 생명 현상에 핵심적인 역할을 하는 미생물의 단백질을 표적으로 한다.
본 연구실에서는 녹농균과 대장균을 각각 병원균과 유익균을 대표하는 미생물 모델로 사용하여, 최신 유전체학, 유전학, 단백질체학, 생화학을 바탕으로 세균의 단백질 항상성에 관여 하는 인자들을 발굴하고, 그 분자적 기전을 규명하는 것을 목표한다. 더 나아가 세균의 단백질 항상성을 타겟으로 하는 미생물 생존 및 감염성 조절 기술 개발을 궁극적인 목표로 연구를 수행하고 있다.
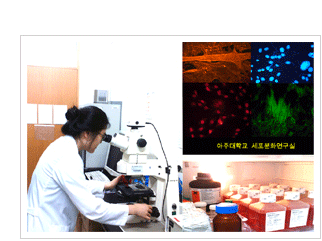
본 연구실에서는 동물 세포의 후기 발생을 조절하는 신호전달기작에 대한 연구를 수행하고 있다. 즉, 최종분화 (terminal differentiation)를 하는 근육 (muscle)을 주 연구대상으로 하여 배양 상태에서 근원세포 (myoblast)가 성장하여 근관조직 (myotube)을 형성하는 과정에서 세포 내외의 조절 인자들과 그들의 작용에 대해 연구하고 있다. 또한 근육은 수축과 이완을 반복하는 조직인데 이를 위해서는 많은 양의 에너지가 필요하다. 그 결과 왕성한 세포호흡 (cellular respiration)으로 인하여 활성산소종 (reactive oxygen species)의 생성이 불가피하고 이로 인해 쉽게 산화스트레스 (oxidative stress)에 노출되는 조직이다. 하지만 근육조직은 이와 같은 산화스트레스에 저항할 수 있는 능력이 있다. 산화스트레스에 의한 세포 내 신호전달기작의 구체적인 작용에 대한 연구를 수행하고 있다. 그리고 산화스트레스는 근육에서 발생하는 치명적인 유전질환인 듀센근위축증 (Duchenne muscular dystrophy)의 진행 과정에서도 중요한 원인으로 작용하는 것으로 알려져 있다. 본 연구실에서는 듀센근위축증의 원인단백질인 디스트로핀과 결합하는 신트로핀 (syntrophin) 단백질을 경유한 신호전달기작에 대한 연구도 병행하고 있다. 한편, 최근에는 의과대학 연구팀과 공동으로 희귀난치성유전질환인 혈우병 (haemophilia)에 대한 연구를 진행하고 있다. 혈우병을 유발하는 응고인자 (coagulation factor VIII & IX)의 유전적 변이에 대한 연구와 효과적인 진단기법을 제안하기 위한 생화학적 연구를 수행하고 있다.

본 연구실은 생명정보학 기술을 이용하여 시스템 수준에서 생명현상을 연구한다. 주로, Omics 데이터에 대한 통계 분석, 머신러닝, 딥러닝의 분석을 수행한다. 예를 들어, 암 조직의 유전체/전사체 분석, 항체 발굴 및 단백질 공학을 위한 유전체 연구, 후성유전체학 등 다양한 바이오 데이터를 분석하고 해석하는 연구를 진행 중이다. 이를 통해, immune repertoire 이해, 질병 바이오마커 발굴, 질병 발생 기작 규명과 같이 자연과학적 기초연구와 공학적 응용 연구를 동시에 수행하고 있다.

본 연구실은 최근 분자생물학의 핵심 연구 분야인 genome의 구조 및 기능 분석에 초점을 맞추고 있다. 연구 방법은 genomics 와 bioinformatics tool을 이용해 다양한 genome database와 genome 분석 프로그램, mutant 및 chemical library들을 활용하여 분자 및 세포 수준에서 총체적인 네트워크를 규명하는 방법으로 접근한다. 주된 연구 테마는 세포제어 물질 생산 유전체 규명 연구 및 응용연구로 세포제어 물질 유전자 및 표적세포 인지-상호작용 관련 유전자, 제어 내성 유전자를 분리하고 그 구조 및 작용기작을 이해하고자 한다. 특히 다양한 미생물에서 toxin-antitoxin 유전체와 자연항생제인 bacteriocin 유전체 발굴 및 기능 분석을 활발히 수행하고 있다. 또한 인간 유전체 연구의 하나로 세포 복제 제어 유전체와 약물대사 유전체의 핵심 유전자들을 발굴하여 이들의 작용기작과 개개인에서의 기능의 차이를 분석하는 비교 유전체적 연구를 수행하고 있다.

본 연구실은 세포분열, 유전, 발생, 분화, 사멸등 기본적 생명 현상에 필수적인 유전체 및 후성유전체의 안정성 유지를 위한 유전체 손상 인식-신호 전달-손상 복구 과정 (sensing, signaling, checkpoint/repair)의 통합조절을 연구한다. 유전체 안정성이란? 세포의 생존과 종의 유지를 위해서는 유전체가 안정적으로 유지되고 딸세포로 전달되어야 한다. 따라서, 모든 생명체는 유전체 안정성을 보존하는 분자 기구를 갖추고 있어, 유전체 손상 인식-신호 전달-손상 복구 과정을 수행한다. 유전체 불안정성 및 관련 질환은? 생명체는 다양한 유전체 손상원(복제 오류, 방사선 등 DNA 손상인자, telomere 마모등)에 노출되어 있다. 유전체 안정성 보존 기구의 기능이 손상되는 경우 유전체의 불안정성(DNA 절단과 변이, 염색체 수와 구조 이상등)이 초래되어, 암, 퇴행성 질환등이 유발될 수 있다. 따라서 유전체 안정성을 조절하는 분자기구의 기능을 적절하게 제어함으로써 관련 질환의 예방 및 치료 효과를 증진시킬 수 있다.
- 1. 유전체 안정성 체크포인트의 분자적 네트워크 구축 및 작용점 발굴: 유전체 안정성 유지에 중요한 분자를 발굴하고, 유전체의 손상인식-신호전달-손상복구 과정 (sensing-signaling-checkpoint/repair)간의 유기적 네트워크를 구축한다.
- 2. 유전체 불안정성 질환의 병인기전 규명 및 표적 발굴: 유전체 안정성 유지의 실패는 염색체의 구조/기능 이상 및 DNA 변이의 축적을 야기하여 유전체 불안정성 질환인, 암/노화 등을 유발한다. 이들 질환의 병인기전을 규명하고 표적 유전자를 발굴한다.
- 3. 유전체 불안정성 질환의 치료 후보물질 개발 및 치료 전략 제시: 유전체 불안정성 질환 치료를 위한 후보물질(화합물/플라즈마)의 작용기전을 연구하여 신개념 치료전략을 제시한다.

본 연구실은 담수, 해양, 하구, 육상 생태계의 다양한 생태학적 현상 들을 에너지 흐름과 물질 순환의 관점에서 연구한다.
- 1. 기본적으로 호수와 하구습지, 논 등에 대한 육수학적인 연구를 수행해 왔는데 특히 지방산과 안정동위원소, 분자생물학적인 기법을 이용한 먹이그물 파악연구를 중점적으로 하고 있다. 먹이그물 파악은 생태계에서 에너지가 어떤 경로로 흘러가는지에 대한 정보를 주고 이는 물질 순환, 부영양화, 독성물질 동태 등 많은 생태계 과정을 이해하는 데 중요하다. 정량적인 먹이그물 파악을 위해 가스 크래마토그래피를 이용한 지방산 분석과 탄소와 질소 안정동위원소 분석 등 바이오마커 연구를 하고 있다.
- 2. 최근에는 분자생물학적인 방법인 T-RFLP를 이용한 식물플랑크톤 군집 및 토양내 동물플랑크톤 군집 분석 방법을 개발하고 있고 또한 물범, 저어새, 수달 등 멸종위기동물종의 배설물에 대한 분석을 통해 먹이 관계 파악 기법을 개발하고 있는 중이다. 이러한 먹이 관계 파악은 생태계 전체의 먹이그물 연구에 중요한 수단이 될 수 있다.
- 3. 우리 연구실에서 최근 관심이 있는 주제 중의 하나는 화학생태학 (Chemical Ecology)이다. 생존에 필요한 물질 이외에 다양한 이차대사물질을 생산하는 육상식물을 중심으로 이들이 이런 이차대사물질을 만들어내는 생태학적 조건이 무엇인지 규명하고자 한다. 많은 식물들이 물리적인 환경요인이나 다른 생물과의 상호작용에 의해 이차대사물질의 합성이 유도되는데 이를 잘 연구하면 약용식물들이 언제 어디에서 어떤 상황에서 유효성분들을 만들어내는지 규명할 수 있다.

본 연구실은 다음과 같은 다양한 연구 활동을 하고 있다.
- 1. TLR : Toll-like receptor (TLR) 는 박테리아를 비롯한 외부 인자들이 인체에 침입하였을 때 가장 먼저 반응을 보이는 면역 시스템이다. 10 여종의 TLR에 의해 각종 항원들이 인식되고 NFkB라는 전사인자를 통해 TNF 등 다양한 사이토카인이 유도된다. 사이토카인들은 복잡한 네트워크를 거쳐 인체 면역 시스템을 활성화함으로써 병원체나 암으로부터 우리 몸을 보호하게 된다.
- 2. G protein : G protein은 생체내 신호, 예를 들면 호르몬이나 신경전달계, 또는 시각, 후각, 미각 등의 감각 수용계, 심지어는 통증, 발생, 분화, 학습과 기억에 이르기까지 다양한 신호전달에 관여하고 있다. 오늘날 존재하는 의약품의 50% 정도가 G protein 신호를 조절함으로써 그 약효를 보이고 있는 점을 감안하면 그 중요성은 아무리 강조해도 지나치지 않다. G protein은 alpha, beta, gamma로 이루어진 heterotrimer 이며 alpha의 기능에 따라 다시 s, i, q, 12 등 4가지 family로 나눈다. 각각의 family는 독자적인 pathway를 통과하여 여러 가지 신호를 매개한다.
- 3. 독성 기전 연구 및 제어 방법 개발 : 분자생물학적 기법 및 오믹스 (omics) 기술을 활용하여 의약품 (암 치료제, 면역 치료제, 항생제, 나노물질 등) 을 비롯한 각종 독성 예측물질들의 독성기전을 분석하고, 시스템생물학을 이용한 네트워크 분석을 통하여 생체 세포에 대한 독성을 미리 예측, 평가, 제어함으로써 녹색성장을 위한 첨단 독성 평가기술을 개발하고 이를 활용하여 국민 건강을 위한 친인간/친환경적 안전성을 확보하고 신규 의약품 개발에 활용할 수 있다.
- 4. Systems Biology : 시스템생물학이란 기존에는 불가능하였던 종합적 21세기형 학문이다. Genomic sequence 를 이용한 genomics, DNA chip을 이용한 transcriptomics, yeast 2 hybrid를 이용한 interactomics, 2-D gel 을 이용한 proteomics 등 종래에는 가능하지 않았던 omics 기술을 사용하여 막대한 양의 생물학적 정보를 산출해 내고, 이들을 종합적으로 활용하여 생물학적 현상을 네트워크상의 총체적 변화로 설명하고자 하는 21세기 학문이다. 생체내 신호전달을 컴퓨터상의 시뮬레이션으로 구성, 설명, 증명함으로써 새로운 기작을 예견하는 미래형 학문이다. 이를 통해 생체내 신호전달 네트워크를 종합적으로 구성하고 신약의 타겟점을 찾아 재구성함으로써 효과적인 신약 개발을 추구할 수 있다.

노화는 모든 생물체들이 겪는 현상이다. 하지만, 인간은 오래전부터 노화 억제 및 수명 연장을 꿈꾸어왔다. 그 결과, 최근 특수 물질을 먹인 동물들이 피부, 간, 근육을 포함한 조직들이 젊어지며 수명이 연장된 사례가 연이어 보고되면서 과학계는 흥분하고 있다. 본 연구실은 체내 미네랄 항상성 변화 관점에서 노화 및 노인성 질병의 원인을 연구한다. 본 연구실에서 개발한 체내 미네랄 항상성 변화를 형광으로 추적 할 수 있는 마우스 시스템을 활용하여, 1) 왜 세포는 노화하는가, 2) 간질환, 3) 악성 육종, 4) 피부 질환을 연구한다. 최종 목표는, 건강하게 오래 사는 삶, 즉, “건강 수명 연장"에 인류적 공헌을 하는 것이다.
*홈페이지:https://bbh82429.wixsite.com/bin-bum-ho


















![담당자에게 메일 보내기[새창열림]](/_resources/kr/img/common/foot_webmaster.gif)